O homem é o responsável por produzir radiação artificial que pode ser proveniente, por exemplo, da construção de instalações nucleares, como as usinas, aceleradores, reatores, dentre outras, mas existe a radiação que é proveniente da própria natureza, as radiações naturais. Essas radiações existem no nosso planeta e são provenientes de alguns minerais e, também, do espaço devido à radiação do Sol e de outras estrelas (radiação cósmica).
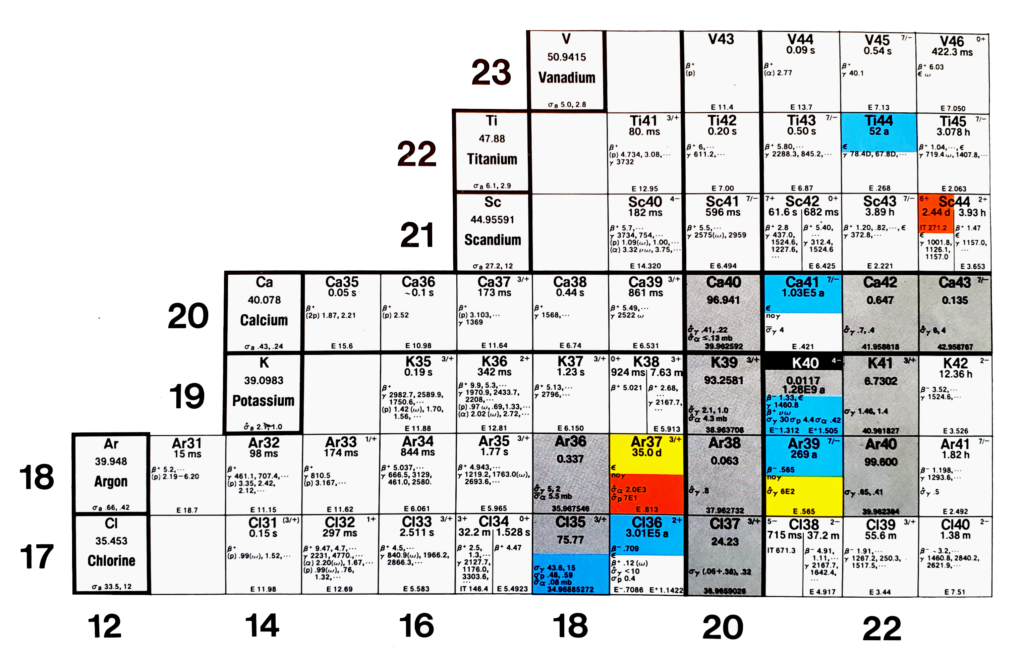
No nosso planeta existem minerais constituídos por elementos químicos que emitem radiações. Os seres humanos, ou melhor, todos os seres vivos têm em seu organismo alguns desses elementos que possuem em sua composição uma porção que emite radiação natural. Como exemplo temos o potássio (K) que está presente em nosso organismo e tem seu componente radioativo expresso pelo isótopo 40K, o que significa que o potássio tem um isótopo naturalmente radioativo.
Isótopo
Considerando que os átomos de um elemento são formados por partículas com carga positiva (prótons), neutra (nêutrons) e negativa (elétrons), o significado do termo isótopo pode ser interpretado por: iso que significa “igual” e tópos que significa “lugar”, ou seja, isótopos de um elemento químico ocupam o mesmo lugar na tabela periódica, o que significa que possuem o mesmo número atômico (Z). Portanto, isótopos são átomos de um mesmo elemento químico que possuem a mesma quantidade de prótons, mas que diferem em número de nêutrons. Quimicamente o potássio é expresso pelo seu número atômico (Z=19) e possui três isótopos: 39K (com 13 nêutrons), 40K (com 14 nêutrons) e 41K (com 15 nêutrons). Esses isótopos possuem as mesmas propriedades químicas, mas diferem em algumas propriedades físicas. Na tabela periódica não é possui obter informações desses isótopos; essas informações são apresentadas na tabela de nuclídeos.
Especificamente o potássio-40 (40K) é um isótopo radioativo (radioisótopo) que possui meia-vida de 1,248 ×109 anos, e está presente no organismo de todos os seres vivos. Da mesma forma, essa radiação natural está presente no solo, nas plantas, nos alimentos, no ar, enfim, no meio ambiente. Essa radiatividade natural resulta na emissão de partículas e/ou radiação.
Outro exemplo de isótopo radioativo natural é o radiocarbono, um isótopo radioativo do elemento carbono, o carbono-14 (14C), cuja meia-vida é de 5,740 anos. O carbono-14 faz parte do ciclo natural do carbono, portanto está presente no gás carbônico (CO2) que é incorporado por todos os seres vegetais e animais. Quando morremos o carbono deixa de ser absorvido e inicia-se uma diminuição da quantidade de 14C no organismo em razão de sua desintegração radiativa, por isso o 14C é usado para datar fósseis.
Considerando a exposição dos seres vivos, tanto à radiação natural quanto artificial, o conhecimento sobre seus efeitos no corpo humano precisa ser estudado, bem como avaliado (monitorado), para evitar que a exposição indevida ou prolongada à radiação cause danos biológicos ou danos ao meio ambiente. A monitoração da radiação natural é usual, por exemplo, em solos e minas que contêm alto teor de elementos naturalmente radioativos, bem como em alimentos produzidos em solos ricos em isótopos radioativos e em materiais de construção como o concreto (contém potássio 40). Essa monitoração é realizada por monitores ou dosímetros, dispositivos utilizados para medir o nível da exposição à radiação em ambientes ou pessoas.
Com relação aos danos biológicos devido a exposição à radiação natural, você não precisa de dosímetro para ficar na praia, é só estar atento aos horários adequados ao banho de sol, caso contrário você vai sentir os danos causados pela radiação solar na sua pele. Entretanto, indivíduos que trabalham em atividades que envolvem a exposição à radiação ionizante precisam usar dosímetro para monitoração individual.
Descoberta da radiotividade natural
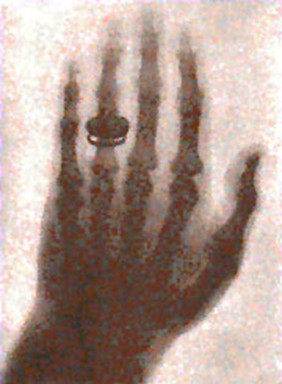
Em 1895 o físico Wilhelm Konrad Röntgen descobriu um tipo de raio que tinha a capacidade de impressionar chapas fotográficas, isto é, permitia que ele visse os ossos de sua mão. Como ele não sabia qual era a natureza desses raios passou a chamá-los de raios X. Na figura pode-se ver a radiografia da mão de sua esposa datada de 1895. É interessante observar que os raios X não atravessaram o metal do anel, mas permite ver os ossos.
Nos anos seguintes muitos experimentos foram realizados com o objetivo de entender os raios X, o que resultou na descoberta de elementos naturalmente radioativos. Um fato relevante a destacar foi a contribuição de Antoine Henri Becquerel que ao investigar minério de urânio identificou um comportamento similar aos raios X, isto é, a radiação que o minério de urânio emitia também tinha a capacidade de impressionar filme fotográfico além de ionizar gases. A explicação viria com os experimentos realizados por Marie Curie e Pierre Curie. Eles passaram a investigar os minérios de urânio e concluíram que todas as substâncias que continham o elemento químico urânio emitiam radiação. Desse modo, o urânio foi o primeiro elemento químico descoberto como sendo naturalmente radioativo. Marie Curie atribuiu a esse fenômeno o termo radioatividade e dando continuidade a seus estudos ela descobriu dois novos elementos químicos, também radioativos, o polônio e rádio. O pouco conhecimento, à época, sobre os efeitos da exposição à radiação levou ao seu uso indevido, como no caso do rádio que passou a ser utilizado em cosméticos, no preparo de tintas luminosas, em bebidas, tônicos, pasta de dentes e muitas outras aplicações que causaram muitas enfermidades como queimaduras, cegueira e até mortes.
Nosso planeta é basicamente água, mas tem sob sua crosta vários isótopos naturalmente radioativos que emitem radiação. Em quantidade suficiente, esses isótopos podem gerar calor e impedir que sua superfície congele totalmente, sendo um dos fatores que permitem a vida no nosso planeta. Isto leva a pensar que se água e a radioatividade natural estiverem presentes em outros planetas, próximos da Via Láctea, teremos planetas candidatos à vida.
Fonte
Klein, C. & Dutrow, B. Manual de Ciência dos Minerais, 23a ed. Bookman, 2012.